Cette nouvelle décision ne manquera pas de susciter de nombreuses interrogations sur l'avenir de la prise en charge de la maladie en France.
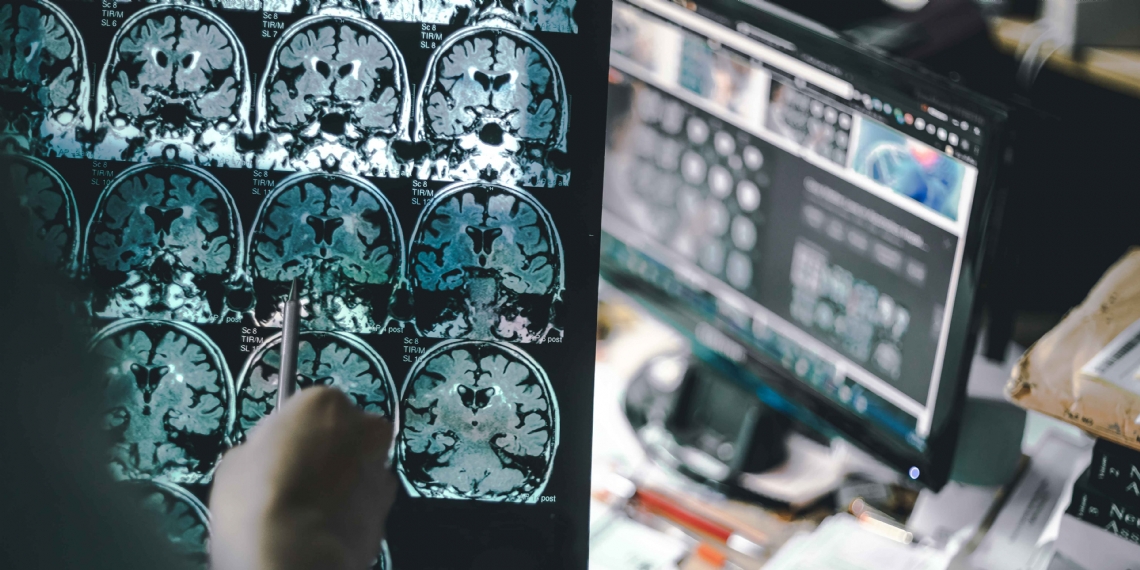

 Alzheimer : après le Leqembi, la HAS refuse l'accès précoce au Kisunla
Alzheimer : après le Leqembi, la HAS refuse l'accès précoce au Kisunla
Cette nouvelle décision ne manquera pas de susciter de nombreuses interrogations sur l'avenir de la prise en charge de la maladie en France.

Pour profiter pleinement de l'ensemble de ses articles, Géroscopie vous propose de découvrir ses offres d'abonnement.
Le 23 octobre, le laboratoire Lilly avait demandé une autorisation d'accès précoce pour la spécialité Kisunla (donanémab), dans le traitement des patients atteints de la maladie d'Alzheimer au stade symptomatique léger (et non porteurs ApoE?4 ou hétérozygote) qui a pourtant obtenu une AMM européenne en novembre 2025, mais non commercialisé en France. L'autorisation d'accès précoce permet aux patients un accès rapide remboursé à des médicaments qui ne sont pas encore autorisés ou pris en charge dans le droit commun.
Dans une décision publiée le 20 mars, le Collège de la Haute autorité de santé (HAS) a refusé cette demande. La commission de transparence a notamment estimé que le médicament « n'est pas susceptible d'être innovant dans l'indication considérée car il ne s'agit pas d'une nouvelle modalité de prise en charge susceptible d'apporter un changement substantiel aux patients en matière d'efficacité ou de qualité de vie, dans la prise en charge actuelle ». Elle note que les données d'efficacité sont issues d'une seule étude de phase III avec des résultats non cliniquement pertinents « dans un contexte où des résultats négatifs en termes de bénéfice clinique chez des patients atteints de maladie d'Alzheimer légère à modérée ont déjà été rapportés au cours du développement de plusieurs autres anticorps anti-amyloïde ».
La décision de non remboursement devrait suivre.
Balance bénéfice/risque
Après réexamen d'une première décision pointant un taux élevé d'effets indésirables sévères (hémorragies et oedèmes cérébraux), l'Agence européenne du médicament avait pourtant jugé favorable la balance bénéfice/risque du Kisunla le 25 juillet 2025 : le laboratoire Lilly avait en effet présenté de nouvelles données montrant un schéma posologique progressif réduisant les effets indésirables. Comme pour le Leqembi, la décision de la HAS ne peut qu'en être plus incompréhensible pour les patients et leurs familles et susciter de nombreuses interrogations sur l'avenir de la prise en charge de la maladie en France. Rappelons que Leqembi (lécanémab), premier anticorps anti-amyloïde évalué par la Commission de transparence de la HAS dans la même indication, s'était également vu refuser cet accès précoce puis son remboursement en novembre dernier, une décision déplorée par les associations de malades, les organismes de recherche, la Société française de gériatrie et gérontologie, la Fédération des centres mémoire et la Société francophone de psychogériatrie et de psychiatrie de la personne âgée.
 Le Défi Ogénie lance sa 3ème édition sur le thème de la photographie
Le Défi Ogénie lance sa 3ème édition sur le thème de la photographie
 Bass : Axess propose la création d'un organisme paritaire de prévention
Bass : Axess propose la création d'un organisme paritaire de prévention
 Audioprothésistes en Ehpad : une question toujours sur la table
Audioprothésistes en Ehpad : une question toujours sur la table
 Prévention : le programme Icope entre enfin dans le droit commun
Prévention : le programme Icope entre enfin dans le droit commun
 BAD : c'est de nouveau non pour l'augmentation des salaires
BAD : c'est de nouveau non pour l'augmentation des salaires
 L'Union des gérontopôles lance son site internet
L'Union des gérontopôles lance son site internet
 Maladies neurodégénératives : premier essai clinique pour le casque de photobiomodulation de Clinatec.
Maladies neurodégénératives : premier essai clinique pour le casque de photobiomodulation de Clinatec.
 Accès aux soins : la crise s'aggrave, la téléconsultation s'impose comme réponse
Accès aux soins : la crise s'aggrave, la téléconsultation s'impose comme réponse
 Chute mortelle dans un Ehpad : deux infirmières comparaissent pour homicide involontaire
Chute mortelle dans un Ehpad : deux infirmières comparaissent pour homicide involontaire
Copyright © 2022 - Tous droits réservés